Lo stress fa ingrassare o dimagrire?

È ormai lo stress il migliore amico dell’uomo moderno: il corpo alza i livelli di cortisolo (definito anche ormone dello stress) in risposta ad una vita frenetica, all’allenamento, ad un’eccessiva restrizione calorica, a tensioni psicologiche come ansia e depressione.
Come influisce questo ormone sulla composizione corporea?
Lo stress fa ingrassare? O, al contrario, lo stress fa dimagrire? E se in realtà fa sia perdere che prendere peso?
Lo stress fa ingrassare?
Lo stress stimola l’appetito: questo meccanismo è perfettamente fisiologico, infatti dal punto di vista evolutivo è sensato integrare le energie dopo un evento stressante. Ora sarà possibile dare la colpa dei chili in più anche alla teoria dell’evoluzione!
Inoltre, il cortisolo da una parte causa anche leptino-resistenza e stimola la fame, dall’altra aumenta la glicemia, che in concomitanza con l’insulinemia elevata porta ad insulino-resistenza: non gestisci più bene i carboidrati.
A livello del tessuto adiposo, il cortisolo stimola sia l’enzima della lipolisi che quello che scinde i trigliceridi, i cui prodotti (acidi grassi) possono o entrare nell’adipocita per accumularsi o essere ossidati. Ci sono delle differenti espressioni di questi enzimi nel tessuto adiposo sottocutaneo e viscerale: lo stress cronico porta ad una ridistribuzione del grasso nella regione addominale viscerale, che aumenta l’infiammazione, predispone a malattie metaboliche e aumenta il rischio cardiovascolare. Inoltre, in sinergia con l’insulina promuove la differenziazione e la proliferazione degli adipociti.
Un altro aspetto interessante e che contribuisce a diminuire il dispendio energetico è l’inibizione della sintesi delle proteine disaccoppianti UCP: queste proteine quando presenti fanno si che l’energia non venga trasformata in ATP ma in calore. Ma se assenti (sintesi inibita) l’energia non viene dispersa in calore.
Lo stress fa dimagrire?
Il cortisolo è un ormone catabolico: ma fermarsi a questa definizione (comunque corretta) è un po’ limitante. È come dire che l’insulina è un ormone anabolico e quindi che faccia ingrassare, a prescindere. Ma è certo che anche chi dimagrisce ha l’insulina e anche ben funzionante. Questo per dire che analizzare un ormone singolarmente non ha molto senso: è importante conoscere il contesto e come l’ormone si comporta in questo insieme ad altri fattori.
Nonostante sia “catabolico” e che quindi potenzialmente possa far perdere peso, il cortisolo in un contesto ipercalorico non intacca la massa muscolare (puoi tirare un sospiro di sollievo. E anche gli addominali).
Lo stress fa gonfiare la pancia?
Il tuo intestino non è solo: in media contiene ben 2 kg di batteri! Questi microrganismi costituiscono la flora batterica intestinale, anche definita microbiota, e sono indispensabili per il corretto funzionamento del tratto digerente.
Le sostanze che non sei in grado di digerire (come l’amido resistente, la fibra alimentare) vengono metabolizzate proprio da questi batteri tramite fermentazione: una reazione che tra i prodotti (es. acidi grassi a catena corta, utili all’organismo) vede anche anidride carbonica (CO2) e idrogeno (H2), entrambi composti gassosi.
Un microbiota alterato è il risultato di abitudini alimentari scorrette (troppi grassi, troppe proteine, poche fibre), infezioni, uso di certi farmaci, ma anche dello stress: questi elementi favoriscono lo sviluppo di ceppi di batteri che peggiorano la permeabilità intestinale, producono sostanze infiammatorie e diabetogene. Che qualcosa non funziona come dovrebbe a livello intestinale può essere evidente anche proprio dalla pancia gonfia, oltre che altri segni di cattivo assorbimento o dolori addominali.
Cortisolo e aumento del peso
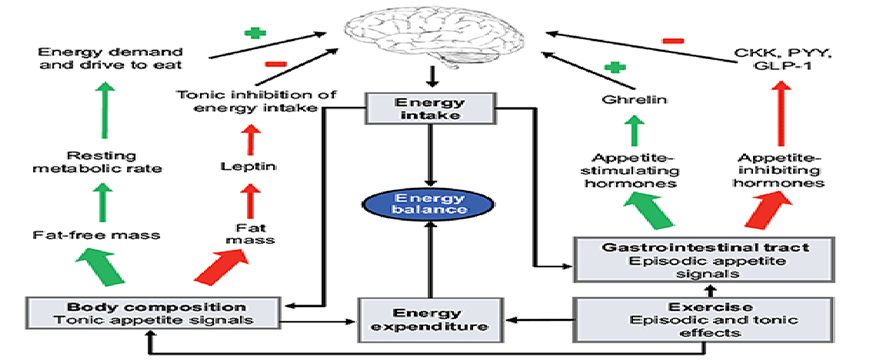
Il cortisolo è uno dei responsabili dell’aumento del peso (nel cronico) perché è anche uno degli ormoni che influenza il centro della fame a livello dell’ipotalamo. Nell’ipotalamo (una parte del sistema nervoso centrale) ci sono neuroni:
- oressigeni (della fame): che vengono inibiti dalla leptina e secernono NPY (il più potente oressigeno endogeno),
- anoressigeni (della sazietà): che producono altri ormoni e vengono stimolati dalla leptina.
Quando questo sistema lavora in fisiologia, c’è una fine regolazione dell’assunzione di cibo che ti porta a mantenere lo stesso peso (omeostasi) per lungo tempo.
Tuttavia, nella società occidentale, c’è una grossa disponibilità di alimenti ricchi di grassi e zuccheri a basso costo (comfort food): cibi che gratificano istantaneamente quando li mangi, anche quando non hai realmente fame. Questo perché viene attivato il circuito dopaminergico del piacere, lo stesso coinvolto nelle dipendenze da alcol e droghe.
Proprio questo meccanismo edonico è fortemente spinto non solo da emozioni negative, ma anche dallo stress cronico: si crea una forte dipendenza dal cibo e il famoso “smetto quando voglio” non è poi così facile da rispettare, se non con una grande forza di volontà.
In questo modo, il cortisolo è complice dell’aumento di peso: ti fa mangiare di più, ti fa cedere di più ai cibi grassi e zuccherini nel cronico. E così, molto probabilmente eccedi rispetto al tuo fabbisogno calorico e ingrassi.
Cortisolo o non cortisolo, alla base di tutto c’è sempre il bilancio energetico.
Tensione nervosa, ansia e dimagrimento da stress: sintomi e rimedi
In riassunto di quanto detto finora, i risultati complessivi di uno stress eccessivo e duraturo sono:
- ipercortisolemia
- iperglicemia
- ridotto dispendio energetico
- bassa tolleranza glucidica
- appetito
- necessità di ingerire cibo caloricamente denso
- infiammazione sistemica più elevata
- ambiente catabolico per il tessuto scheletrico in particolare
- ambiente neutro o anabolico per il tessuto adiposo
Sapere in anticipo se e quando il fisiologico meccanismo che regola lo stress diventa patologico è impossibile perché l’epigenetica influenza moltissimo la risposta individuale: ecco perché una minoranza di persone in risposta allo stress cronico perde peso.
Come hai appena letto, la situazione complessiva che si instaura non è propriamente delle più rosee. Cosa fare?
- Trova il modo migliore di ridurre o, ancora meglio, eliminare il fattore stressante per interrompere il circolo vizioso
- Evita approcci alimentari drastici
- Riduci il volume e l’intensità dell’allenamento per non esacerbare gli effetti del cortisolo e non sovraccaricare ulteriormente il sistema nervoso
- Non porti obbiettivi specifici o PR da raggiungere in un periodo molto stressante, conserva le energie
- Prova attività alternative che favoriscano il recupero psico-fisico (cardio LISS per tempi brevi, yoga, tecniche di meditazione)
- Evita stimolanti come caffè, guaranà, tè, termogenici, sinefrina
- Dormi bene e riposati abbastanza
- Se non riesci a superare i periodi più stressanti è utile chiedere consiglio ad un medico per eventuali terapie farmacologiche mirate e/o psicoterapiche
Conclusioni: lo stress fa dimagrire o ingrassare?
La risposta individuale, come sempre, conta: c’è chi ha un’alta soglia di sopportazione del cortisolo, chi una più bassa, chi dimagrisce e chi ingrassa. Tendenzialmente, è più facile ingrassare quando sei stressato nel cronico: lo stress agisce a livello sistemico creando una situazione generale che ti induce a mangiare di più e a peggiorare il metabolismo.
Co-autore: dott.ssa Lucia Ienco
Laureata in Biotecnologie e studentessa magistrale di Scienze dell’Alimentazione. Articolista InVictus ed esordiente di weightlifting a livello agonistico.
Approfondisci l’argomento dieta, dimagrimento e ricomposizione corporea, con la nostra guida gratuita per cominciare a farti delle solide basi su cui poi approfondire:
Letteratura consultata :
- Maniam J, Morris MJ (2012) The link between stress and feeding behaviour. Neuropharmacology 63: 97-110.
- Spencer SJ, Tilbrook A (2011) The glucocorticoid contribution to obesity. Stress 14: 233-246.
- Sominsky L, Spencer SJ (2014) Eating behavior and stress: a pathway to obesity. Front Psychol 5: 434.
- Papadimitriou A, Priftis KN (2009) Regulation of the hypothalamic-pituitary-adrenal axis. Neuroimmunomodulation 16: 265-271.
- Schneeberger M, Gomis R, Claret M (2014) Hypothalamic and brainstem neuronal circuits controlling homeostatic energy balance. J Endocrinol 220: T25-46.
- Berridge KC (2009) ‘Liking’ and ‘wanting’ food rewards: brain substrates and roles in eating disorders. Physiol Behav 97: 537-550.
- Volkow ND, Wang GJ, Baler RD (2011 Reward, dopamine and the control of food intake: implications for obesity. Trends CognSci 15: 37-46.
- Monteleone P, Maj M (2013) Dysfunctions of leptin, ghrelin, BDNF and endocannabinoids in eating disorders: beyond the homeostatic control of food intake. Psychoneuroendocrinology 38: 312-330.
- Liu S, Borgland SL (2015) Regulation of the mesolimbic dopamine circuit by feeding peptides. Neuroscience 289: 19-42.
- Pecoraro N, Reyes F, Gomez F, Bhargava A, Dallman MF (2004) Chronic stress promotes palatable feeding, which reduces signs of stress: feedforward and feedback effects of chronic stress. Endocrinology 145: 3754-3762.
- Jéquier E (2002) Leptin signaling, adiposity, and energy balance. Ann NY AcadSci 967: 379-388.
- Asensio C, Muzzin P, Rohner-Jeanrenaud F (2004) Role of glucocorticoids in the physiopathology of excessive fat deposition and insulin resistance. Int J ObesRelatMetabDisord 28 Suppl 4: S45-52.
- Suzuki K, Simpson KA, Minnion JS, Shillito JC, Bloom SR (2010) The role of gut hormones and the hypothalamus in appetite regulation. Endocr J 57: 359-372.
- Macfarlane DP, Forbes S, Walker BR (2008) Glucocorticoids and fatty acid metabolism in humans: fuelling fat redistribution in the metabolic syndrome. J Endocrinol 197: 189-204.
- Slavin BG, Ong JM, Kern PA (1994) Hormonal regulation of hormone-sensitive lipase activity and mRNA levels in isolated rat adipocytes. J Lipid Res 35: 1535-1541.
- Arvaniti K, Ricquier D, Champigny O, Richard D (1998) Leptin and corticosterone have opposite effects on food intake and the expression of UCP1 mRNA in brown adipose tissue of lep(ob)/lep(ob) mice. Endocrinology 139: 4000-4003.
- Benker G, Raida M, Olbricht T, Wagner R, Reinhardt W, et al. (1990) TSH secretion in Cushing’s syndrome: relation to glucocorticoid excess, diabetes, goitre, and the ‘sick euthyroid syndrome’. ClinEndocrinol (Oxf) 33: 777-786.
- Mullur R, Liu YY, Brent GA (2014) Thyroid hormone regulation of metabolism. Physiol Rev 94: 355-382.
- Grasselli E, Canesi L, Voci A, De Matteis R, Demori I, et al. (2008) Effects of 3,5-diiodo-L-thyronine administration on the liver of high fat diet-fed rats. Exp Biol Med (Maywood) 233: 549-557.
- Grasselli E, Voci A, Demori I, Canesi L, De Matteis R, et al. (2012) 3,5-Diiodo-L-thyronine modulates the expression of genes of lipid metabolism in a rat model of fatty liver. J Endocrinol 212: 149-158.
- Schleimer RP (1993) An overview of glucocorticoid anti-inflammatory actions. Eur J Clin Pharmacol 45 Suppl 1: S3-7.
- Silverman MN, Sternberg EM (2012) Glucocorticoid regulation of inflammation and its functional correlates: from HPA axis to glucocorticoid receptor dysfunction. Ann NY AcadSci 1261: 55-63.
- Wisse BE (2004) The inflammatory syndrome: the role of adipose tissue cytokines in metabolic disorders linked to obesity. JASN 15: 2792-2800.
- Fontana L, Eagon JC, Trujillo ME, Scherer PE, Klein S (2007) Visceral fat adipokine secretion is associated with systemic inflammation in obese humans. Diabetes 56: 1010-1013.